Les selenoproteïnes formen un grup de proteïnes que incorporen l'aminoàcid número 21, la selenocisteïna (Sec), un anàleg de cisteïna que conté seleni enlloc de sofre. Aquest aminoàcid ve codificat pel codó UGA, que normalment s'interpreta com stop codon. En eucariotes, aquesta recodificació és possible per l'estructura secundària que adquiereix l'mRNA gràcies a un motiu en cis situat al seu 3'-UTR, anomenat element SECIS (SElenoCystein Insertion Sequence).
 Esquema general i exemples d'elements SECIS de diverses selenoproteïnes. Extret de Kryukov GV, et al.
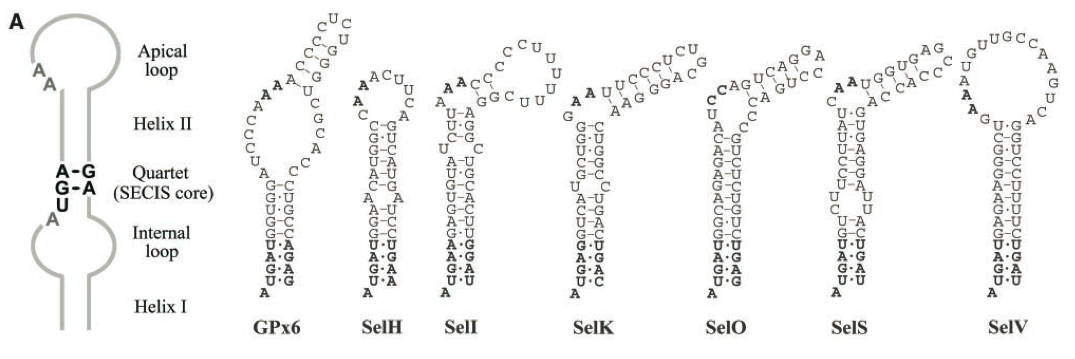
Esquema general i exemples d'elements SECIS de diverses selenoproteïnes. Extret de Kryukov GV, et al.
La síntesi de selenocisteïna requereix proteïnes específiques com són la selenofosfat sintetasa (SPS1 i SPS2), la selenocisteïna sintasa (SLA/LP), la fosfoseril tRNA quinasa (PSTK) i la proteïna associada a selenocisteïna (SECP43). Per altra banda, la incorporació de l'aminoàcid precisa l'acoblament d'un conjunt de factors específics que actuen en trans (SBP2, eEFsec, un tRNA específic).
 Esquema general del procés de síntesi de selenocisteïna en eucariotes. Extret de Allmang C, et al.
Esquema general del procés de síntesi de selenocisteïna en eucariotes. Extret de Allmang C, et al.
Tot i que el seleni és un nutrient essencial en animals, microorganismes i altres eucariotes, la funció de les selenoproteïnes no sempre és clara. En humans s'ha associat la deficiència de seleni amb la malaltia de Keshan, trastorn en què destaca una necrosi miocàrdica que porta a debilitat cardíaca (Lobanov AV, et al.).
La majoria de selenoproteïnes són enzims redox que semblen actuar com a antioxidants on la selenocisteïna és el residu catalític (és altament nucleofílic). Existeixen ortòlegs que incorporen cisteïnes enlloc de selenocisteïnes, tot i presentar menors activitats catalítiques (amb algunes excepcions, com sempre en biologia). Tenint en compte que S i Se tenen la mateixa configuració electrònica a les darreres capes de valència (per això es troben al mateix grup de la taula periòdica) sembla comprensible que ambdós elements siguin relativament intercanviables en els aminoàcids d'aquestes proteïnes.